একটি কোষে যতো রাসায়নিক বিক্রিয়া ঘটে তাদের একসাথে বলে মেটাবোলিজম (Metabolism)। এই বিক্রিয়াগুলোকে দুটিভাগে ভাগ করা যায়। অপচিতি বা ক্যাটাবোলিজম (Catabolism) এবং উপচিতি বা এনাবোলিজম (Anabolism)। এই রাসায়নিক বিক্রিয়াগুলো পরস্পর সম্পর্কযুক্ত, অনেকটা বিশাল কোনো মেট্রোরেল নেটওয়ার্কের মতো। কোষের বিভিন্ন পাথওয়ে (Pathway) বা প্রক্রিয়াগুলো একাধিক রাসায়নিক বিক্রিয়া ব্যবহার করে তাদের কাজ সম্পাদন করে। পাথওয়েগুলোতে এক বিক্রিয়ায় সৃষ্ট উপাদান অন্য বিক্রিয়ায় বিক্রিয়ক (Reactant) হিসেবে ব্যবহৃত হয়। ক্যাটাবোলিক বিক্রিয়াগুলো জটিল উপাদানকে ভেঙ্গে সরল উপাদানে পরিণত করে। এই ক্যাটাবোলিক পাথওয়েগুলো এক্সার্গনিক (Exergonic), অর্থাৎ, এতে শক্তির নির্গত হয়। অন্যদিকে, এনাবোলিক বিক্রিয়ায় কোষ সরল উপাদান থেকে দরকারী জটিল উপাদান, যেমন: প্রোটিন, নিউক্লিইক-অ্যাসিড, লিপিড ইত্যাদি তৈরি করে। এনাবোলিক বিক্রিয়াগুলো এন্ডোর্গনিক (Endergonic)। অর্থাৎ, এই বিক্রিয়াগুলো শক্তি শোষণ করে। এনাবোলিক বিক্রিয়াগুলো এই শক্তি পায় ক্যাটাবোলিক বিক্রিয়া থেকে। কিন্তু, বেশিরভাগ ক্যাটাবোলিক বিক্রিয়ায় শক্তি তাপ হিসেবে বের হয়ে যায়। আমাদের দেহকোষে তিন ধরণের ক্যাটাবোলিক পাথওয়ে রয়েছে, গ্লাইকোলিসিস (Glycolysis), ক্রেব-সাইকেল (Krebs cycle), এবং ETC বা ইলেক্ট্রন-ট্রান্সপোর্ট-চেইন (Electron transport chain) যেগুলো থেকে প্রাপ্ত শক্তি এনাবোলিক পাথওয়েতে ব্যবহার করা যায়।
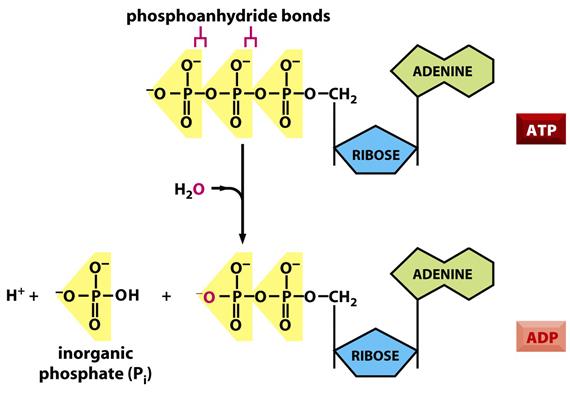
বর্ণিত ক্যাটাবোলিক পাথওয়ে তিনটি থেকে এনাবোলিক পাথওয়েতে শক্তি স্থানান্তরিত হয় একটি বিশেষ অণুর মাধ্যমের নাম ATP বা এডেনোসিন-ট্রাইফসফেট (Adenosine triphosphate)। ATP আসলে তিনটি ফসফেট-গ্রুপযুক্ত এডেনিন নিউক্লিইক-অ্যাসিড। ফসফেট-গ্রুপে রয়েছে একটি ফসফরাস এবং চারটি অক্সিজেন পরমাণু। ATP তার শক্তি ধরে রাখে এই ফসফেট-গ্রুপগুলোর বন্ধনগুলোর মধ্যে, এই বন্ধনকে বলে ফসফোয়নহাইড্রাইড বন্ধন (Phosphoanhydride)। ATP হাইড্রোলাইসিস (Hydrolysis) এনজাইমের মাধ্যমে তার শেষপ্রান্তের ফসফেট-গ্রুপটি হারিয়ে পরিণত হয় ADP বা এডেনোসিন-ডাইফসফেটে (Adenosine diphosphate)। অন্যদিকে, মুক্ত অজৈব ফসফেট-গ্রুপটি (Pi) যুক্ত হয় অন্য কোনো বিক্রিয়কের সাথে। এই ফসফেট-গ্রুপ যুক্তকরণ প্রক্রিয়াকে বলে ফোসফোরেলেশন (Phosphorylation)। ফোসফোরেলেশন প্রক্রিয়ায় বিক্রিয়ক এন্ডোর্গনিক বিক্রিয়া শুরু করার মতো যথেষ্ট শক্তি পেয়ে থাকে। যেখানই শক্তির প্রয়োজন কোষ সেখানেই ATP ব্যবহার করে। এই ATP কোষের শক্তি মুদ্রা। এক হিসেবে অনুসারে, একটি সংকুচিত হতে থাকা মাংসপেশী প্রতি সেকেন্ডে ব্যবহার করে প্রায় ১০মিলিয়ন ATP। ৬ফিট লম্বা একজন পুরুষ প্রতিদিন প্রায় ৮২কেজি ATP ব্যবহার করে। সু-সংবাদ হলো, ATP একটি নবায়নযোগ্য মুদ্রা, অর্থাৎ, ATP-কে রিচার্জ করা সম্ভব। ATP ফসফেট-গ্রুপ হারিয়ে ADP-যে পরিণত হয়, এই ADPগুলোই পরবর্তীতে কোনো এনজাইমের কল্যাণে ফসফোরেলেশনের মাধ্যমে আবার ATP-তে রূপান্তরিত হয়। এই এনজাইমগুলোকে বলে কাপলিং-এনজাইম (Coupling enzyme)।
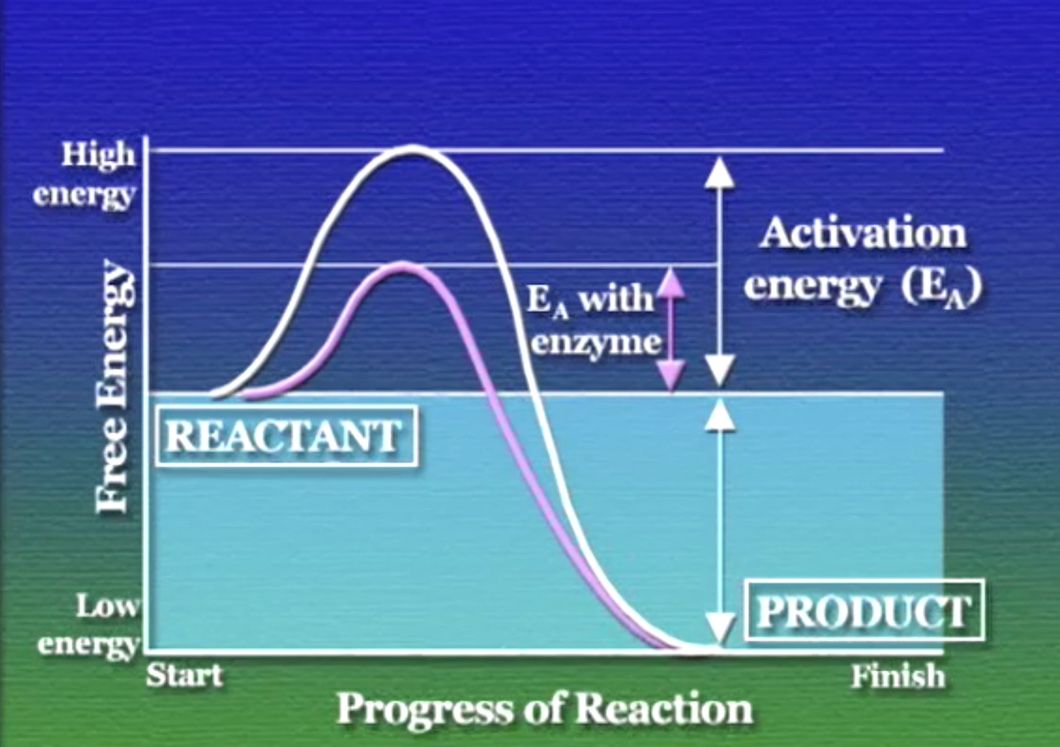
ফোসফোরেলেশন মূলত এন্ডোর্গনিক বা শক্তি-শোষক বিক্রিয়াগুলোকে এক্সার্গনিক বা শক্তি-দায়ক বিক্রিয়ায় রূপান্তরিত করে। কিন্তু, এক্সার্গনিক বিক্রিয়াগুলো কখনোই স্বতঃস্ফূর্তভাবে শুরু হয় না। অনেকটা মোমবাতির মতো, মোমবাতি নিজে থেকেই স্বতঃস্ফূর্তভাবে জ্বলে ওঠে না। কিন্তু, একবার যদি জ্বালিয়ে দেয়া হয় তবে মোমবাতি নিজে নিজেই কারো সাহায্য ছাড়াই জ্বলতে থাকবে। থার্মোডিনামিক্সের ভাষায় এই অবস্থাকে বলে, মেটাস্ট্যাবল (Metastable) বা স্বল্প-সুস্থিত অবস্থা। সাধারণত অজৈব বিক্রিয়ার ক্ষেত্রে আমরা তাপ প্রয়োগের মাধ্যমে বিক্রিয়কদের মেটাস্ট্যাবল অবস্থা থেকে বের করে আনি, যাতে বিক্রিয়া শুরু হতে পারে। যেকোনো বিক্রিয়া শুরুর জন্য এই প্রারম্ভিক শক্তিকে বলে এক্টিভেশন-এনাৰ্জি (Activation energy)। কিন্তু, কোষের মেটাবোলিক পাথওয়ের বিক্রিয়াগুলোর এক্টিভেশন-এনাৰ্জি এতোই বেশি যে, এই বিক্রিয়া শুরু করা জন্য প্রচুর তাপের দরকার। এতে কোষ নিজেই পুড়ে কাবাব হয়ে যাবে। নিজেকে বাঁচানো ছাড়াও কোষকে আরেকটা কাজ করতে হয়, সেটা হলো নিয়ন্ত্রণ। অপ্রয়োজনে কোনো বিক্ৰিয়া চালানো কোষের জন্য অপচয়। যেকোনো বিক্রিয়া শুরু এবং নিয়ন্ত্রণের জন্য কোষ ব্যবহার করে জৈব অনুঘটক বা ক্যাটালিস্ট (Catalyst)। এই জৈব অনুঘটকদের আমরা বলি এনজাইম (Enzymes)।


এনজাইমেরা হলো প্রোটিন। যেকোনো প্রোটিনের মতোই এনজাইদের কাজ নির্ভর করে তাদের আকারের ওপর। প্রতিটি এনজাইমের কিছু বিশেষ অংশ আছে যেখানে বিক্রিয়কেরা এসে যুক্ত হয়। এই অংশগুলোকে বলে এক্টিভ-সাইট (Active site) আর বিক্রিয়কদের বলে সাবস্ট্রেট (Substrate)। প্রতি এক্টিভ-সাইটের একটা সুনির্দিষ্ট আকার আছে, তাই চাইলেও যেকোনো সাবস্ট্রেট এনজাইমের এক্টিভ-সাইটে যুক্ত হতে পারে না। অনেকটা তালা-চাবির মতো। আবার অনেক এক্টিভ-সাইট কিছুটা নমনীয়। সাবস্ট্রেট যুক্ত হবার সাথে সাথে নিজেদের আকার অল্প-বিস্তর পরিবর্তন করে এরা সাবস্ট্রেটকে যুৎসই মতো আটকে ফেলে। এক্টিভ-সাইটের এই নমনীয়তাকে বলে ইন্ডিউসড-ফিট (Induced fit)। প্রয়োজনীয় সাবস্ট্রেটেরা এক্টিভ-সাইটগুলোতে যুক্ত হলে, এনজাইমেরা এই সাবস্ট্রেটগুলোকে কাছাকাছি এবং সঠিক অবস্থানে নিয়ে আসে। এরপর এনজাইমেরা সাবস্ট্রেটগুলোকে বাঁকাতে, মচকাতে শুরু করে। এই বাকাঁনি, মচকানি, এবং এক্টিভ-সাইটগুলোর বৈদ্যুতিক ও রাসায়নিক বৈশিষ্ট্যের কারণে সাবস্ট্রেটগুলোর এক্টিভ-এনাৰ্জির পরিমাণ কমে যায় এবং বিক্রিয়া শুরু হয়। আর, বিক্রিয়া শেষ হলে সাবস্ট্রেটগুলো খসে পরে এবং নতুন সাবস্ট্রেট এসে যুক্ত হয়। এক হিসাব অনুসারে, কিছু কিছু প্রোটিনের পেপটাইড-চেইনের শেষে একটা আরজিনিন (Arginine) অ্যামিনো অ্যাসিড থাকে, যাকে প্রোটিন প্রক্রিয়াজাতকরণ পর্যায়ে ছেঁটে ফেলতে হয়। এই ছেঁটে ফেলার কাজটি করে কার্বোক্সিপেপ্টাইডেস-এ (Carboxypeptidase A) নামের এক এনজাইম। পেপটাইড-চেইনে এই আরজিনিনের পেপটাইড-বন্ধনের হাফ-লাইফ (Half life) বা অর্ধ-জীবন প্রায় ৭বছর। অর্থাৎ, যদি ২০টি পেপটাইড-চেইনকে রেখে দেয়া হয় তবে, ৭বছর পর প্রায় ১০টি চেইন থেকে পেপটাইড-বন্ধন ভেঙ্গে আরজিনিন স্বতঃস্ফূর্তভাবে বেরিয়ে যাবে। আরো ৭বছর পর বাকি চেইনগুলোর অর্ধেক, প্রায় ৫টি তাদের আরজিনিন হারাবে। কিন্তু, কার্বোক্সিপেপ্টাইডেস-এ এনজাইমটি এই আরজিনিনকে ছেঁটে ফেলে মাত্র অর্ধ-সেকেন্ডে। অর্থাৎ, এনজাইমেরা বিক্রিয়া শুধুই শুরু করেনা, বরং দ্রুততর করে।
আগে বলা হয়েছিলো, মেটাবোলিক পাথওয়েগুলোতে একাধিক বিক্রিয়া প্রয়োজন। এই বিক্রিয়াগুলোর একটির উৎপাদিত বস্তু অন্য বিক্রিয়ার সাবস্ট্রেট হিসেবে ব্যবহৃত হয়। এবং প্রতিটি বিক্রিয়ায় এক বা একাধিক এনজাইম অনুঘটক হিসেবে কাজ করে। কোষ কোনো নির্দিষ্ট মেটাবোলিক পাথওয়ের প্রতিটি বিক্রিয়াকে একে একে নিয়ন্ত্রণ না করে বরং ঐ পাথওয়ের পুরোটাকেই একসাথে নিয়ন্ত্রণ করে। যেমন: থ্রেয়নিন (Threonine) থেকে আইসোলুসিন (Isoleucine) পেতে পাঁচটি বিক্রিয়া পেরুতে হয়, এবং প্রতিটি বিক্রিয়ায় রয়েছে একটি করে এনজাইম। শেষ ধাপে যখন আইসোলুসিন তৈরি হয়, এই আইসোলুসিন গিয়ে যুক্ত হয় প্রথম বিক্রিয়ায় সাহায্যকারী এনজাইমের একটা নির্দিষ্ট অংশের সাথে, এই অংশটা কিন্তু এক্টিভ-সাইট নয়। আইসোলুসিন আটকে যাওয়ায় এনজাইমটি নিক্রিয় হয়ে পরে। ফলে, পুরো পাথওয়ে আর কোনোভাবেই পরবর্তী বিক্রিয়ায় যেতে পারে না। অর্থাৎ, মেটাবোলিক পাথওয়েগুলোর চূড়ান্ত উৎপাদিত বস্তুই ঐ পাথওয়েগুলোকে নিয়ন্ত্রণ করে। এই নিয়ন্ত্রণ প্রক্রিয়াকে বলে ফিডব্যাক-ইনহিবিশন (Feedback inhibition)।

ক্যাটাবোলিক পাথওয়েগুলোর মধ্যে গ্লাইকোলিসিস এবং ক্রেব-সাইকেলকে বলা যায় কোষের দহন প্রক্রিয়া। এই দহন প্রক্রিয়ায় কোষ গ্লুকোস পুড়িয়ে শক্তি উৎপন্ন করে। এই ক্যাটাবোলিক পাথওয়েগুলোর বিক্রিয়াগুলোকে তাই বলা হয় বলে অক্সিডেশন-রিডাকশন বিক্রিয়া (Oxidation and reduction), সংক্ষেপে রিডক্স (Redox)। । অক্সিডেশন বিক্রিয়ায় সাবস্ট্রেটগুলো ইলেট্রন হারাতে থাকে। চূড়ান্ত ধাপে এই ইলেক্ট্রনগুলো যুক্ত হয় অক্সিজেনের সাথে। অক্সিজেনের কাছে ইলেক্ট্রন হারাবার কারণে এই বিক্রিয়াগুলোকে বলে অক্সিডেশন। অন্যদিকে, রিডাকশন বিক্রিয়ায় সাবস্ট্রেটগুলোতে নেগেটিভ চার্জযুক্ত ইলেক্ট্রন যুক্ত হতে থাকে। ফলে, সাবস্ট্রেটগুলোর পজিটিভ চার্জ কমতে থাকে, তাই এদের বলে রিডাকশন। একটি রিডক্সে বিক্রিয়ায় অক্সিডেশন এবং রিডাকশন একসঙ্গে চলতে থাকে। অর্থাৎ, যদি একটি বিক্রিয়ক অক্সিডাইজড হয় তবে অপর বিক্রিয়ক রিডউসড হয়।
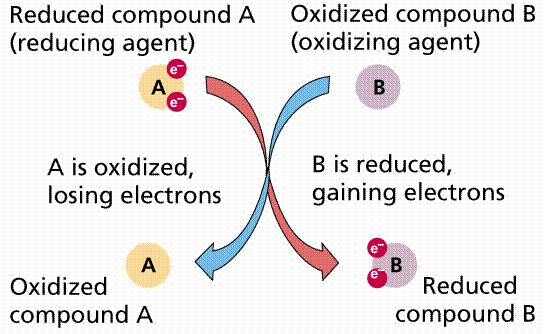
এবার রিডক্স বিক্রিয়ার ইলেক্ট্রনের উৎসের দিকে তাকানো যাক। কোষ মূলত গ্লুকোসকে ভেঙে শক্তি তৈরি করে। এই গ্লুকোসে ছয়টি কার্বন এবং ছয়টি অক্সিজেন রয়েছে। কার্বন একটি অপেক্ষাকৃত কম ইলেক্ট্রোনেগেটিভ (Electronegative) মৌল, পাউলির ইলেক্ট্রোনেগেটিভ স্কেল অনুসারে কার্বনের মান ২.৫৫। এর মানে হলো, কার্বন তার ইলেক্ট্রনগুলোকে দুর্বলভাবে ধরে রাখে। অন্যদিকে, অক্সিজেন তার ইলেক্ট্রনগুলোকে খুবই শক্ত করে ধরে রাখে। ইলেক্ট্রন যদি একবার অক্সিজেনের কক্ষপথে আটকা পরে তবে আর ছাড়াছাড়ি নেই। এইজন্য, অক্সিজেন কার্বনের তুলোনায় বেশি ইলেক্ট্রোনেগেটিভ, এর মান ৩.৪৪। মজার ব্যাপার হলো, যদিও গ্লুকোসে সমপরিমাণ কার্বন এবং অক্সিজেন রয়েছে, কিন্তু, গ্লুকোসের আকৃতি বা কাঠামোর জন্য অক্সিজেনেরা কার্বনের ইলেক্ট্রনগুলোকে ছিনিয়ে নিতে পারেনা। কোষ মূলত অক্সিডেশন বিক্রিয়ায় গ্লুকোসে এই কাঠামো ভেঙ্গে কার্বনের ইলেক্ট্রনগুলো অক্সিজেনকে দিয়ে দেয় এবং এতে যে শক্তি উৎপন্ন হয় তার কিছু অংশ ATP রিচার্জ করতে সাহায্য করে। কার্বন থেকে অক্সিজেনে এই ইলেক্ট্রন স্থানান্তর কিন্তু এক ধাপে হয় না। কোষ এই ইলেক্ট্রন স্থানান্তরের জন্য ব্যবহার করে একধরণের বিশেষ অণু, যাদের বলে ইলেক্ট্রন-বাহক বা ইলেক্ট্রন-ক্যারিয়ার (Electron carriers)। এই ইলেক্ট্রন-ক্যারিয়ারেরা কার্বন থেকে একটু বেশি ইলেক্ট্রোনেগেটিভ ফলে, এরা কার্বন থেকে ইলেক্ট্রন ছিনিয়ে নিতে পারে। কিন্তু, ইলেক্ট্রন-ক্যারিয়ারেরা অক্সিজেন থেকে একটু কম ইলেক্ট্রোনেগেটিভ, ফলে অক্সিজেনের সংস্পর্শে এরা অক্সিজেনের কাছে ইলেক্ট্রন হারায়।
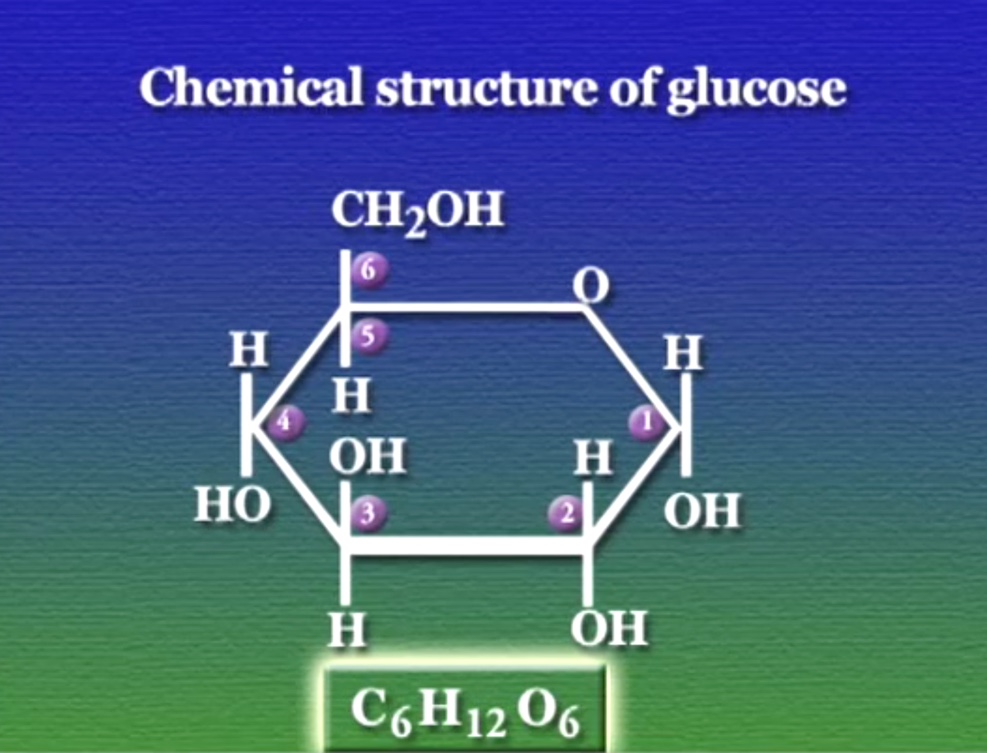

কোষ প্রধানত দুইটি ইলেক্ট্রন-ক্যারিয়ার ব্যবহার করে। NAD বা নিকোটিনামাইড-এডেনিন-ডাইনিউক্লিয়টাইড (Nicotinamide adenine dinucleotide) এবং FAD বা ফ্ল্যাভিন-এডেনিন-ডাইনিউক্লিয়টাইড (Flavin adenine dinucleotide)। মজার বিষয় হলো, NAD গঠনগত ভাবে ATP-এর মতোই। পার্থক্য হলো, NAD-এর তিনটির বদলে দুটি ফসফেট-গ্রুপ রয়েছে, আরও রয়েছে বাড়তি একটা পেন্টোজসুগার এবং একটা নিকোটিনামাইড-গ্রুপ। এই নিকোটিনামাইড-গ্রুপের মাধ্যমেই NAD ইলেক্ট্রন বহনে করে। অক্সিডেশন বিক্রিয়ায় যখন NAD ইলেক্ট্রন হারায় তখন একে বলে NAD+, আর যখন রিডাকশন বিক্রিয়ায় ইলেক্ট্রন লাভ করে তখন একে বলে NADH। FAD-এরও একই অবস্থা, ইলেক্ট্রন শূন্য বা অক্সিডাইজড অবস্থাকে বলে FAD+ এবং ইলেক্ট্রন ভর্তি বা রিডউসড অবস্থাকে বলে FADH2। NAD-কে রিডক্সে সাহায্য করে একটা এনজাইম,নাম ডিহাইড্রোজেনাস (Dehydrogenase)। ডিহাইড্রোজেনাস তার সাবস্ট্রেট থেকে হাইড্রজেন পরমাণু ছিনিয়ে নিয়ে NAD অক্সিডেশন কিংবা রিডাকশনে সাহায্য করে। NADH এবং FADH-এর ইলেক্ট্রনগুলোতে প্রচুর শক্তি থাকে, কিন্তু, কোষ এদের ATP-এর মতো শক্তির উৎস হিসেবে ব্যবহার করতে পারে না। বরং, ইলেক্ট্রন-ক্যারিয়ারগুলো প্রধানত ETC পাথওয়েকে এই উচ্চশক্তির ইলেক্ট্রনগুলোকে সরবরাহ করে।

জীবনের যদি জ্বালানির দরকার হয়, তবে জীবন কি? অনেকের মতে, বিশৃঙ্খল পরিবেশ থেকে নিজেদের আলাদা করে নেয়া এই মেটাবোলিক প্রক্রিয়াগুলোর সমষ্টিই হলো জীবন।
অবলম্বনে: “The Great Courses” থেকে প্রকাশিত “Biology: The Science of Life” by “Stephen Nowicki”